


一、MAH業務介紹
藥品上市許可持有人是指取得藥品注冊證書的企業或者藥品研制機構等。
藥品上市許可持有人制度(MAH)的核心內容是藥品批準文號和生產許可脫離,允許試點的藥品研發機構和科研人員取得藥品的批準文號,并且對藥品質量承擔相應的責任。MAH出臺之前,我們國家實行的是上市許可和生產許可統一捆綁的管理模式,只有生產企業才可以來申請藥品注冊,取得最終的藥品批準文號。
MAH制度出臺之前,我國也有相似的制度:委托生產制度和技術轉讓制度。
值得注意的是,委托生產制度并不是生產許可和上市許可唯一準入制度下面的一個產物,根據現在的委托生產的規定,只能委托生產企業有這個批準文號的企業來委外,也是委托方和受托方均為生產企業,而且本身的批準文號是不隨委托進行變更的。可以說,委托生產本身只是在持有企業擁有技術改造等不具備生產條件下的暫時性的安排。
MAH在國際社會其實早已通行,主流的發達國家和地區普遍采取了藥品上市許可持有人制度。
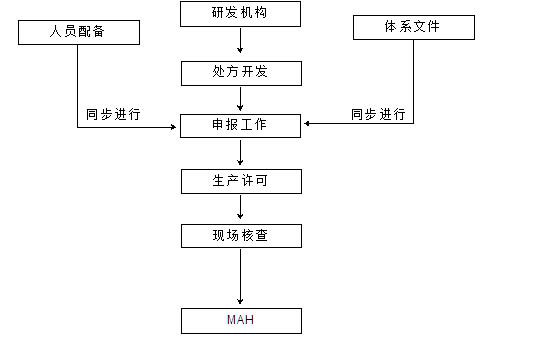
二、項目工作流程
我公司作為第一批較早取得生產許可的研發機構,依托專業的實驗室及認證咨詢團隊,具備豐富的申報經驗。針對不同類型的客戶,可提供定制化服務,幫助客戶建立或優化質量管理體系,優化人員配置,打通申報通道,使得客戶能夠在最短的時間內取得藥品生產許可。
三、成為藥品上市許可持有人需要準備的資料清單一覽
藥品上市許可持有人委托他人生產的情形
1.藥品生產許可證申請表;
2.基本情況,包括企業名稱、擬生產品種、劑型、工藝及生產能力(含儲備產能);
3.營業執照(申請人不需要提交,監管部門自行查詢);
4.組織機構圖(注明各部門的職責及相互關系、部門負責人);
5.法定代表人、企業負責人、生產負責人、質量負責人、質量受權人及部門負責人簡歷、學歷、職稱證書和身份證(護照)復印件;依法經過資格認定的藥學及相關專業技術人員登記表,并標明所在部門及崗位;高級、中級、初級技術人員的比例情況表;
6.擬委托生產的范圍、劑型、品種、質量標準及依據;
7.擬委托生產劑型及品種的工藝流程圖,并注明主要質量控制點與項目、受托方共線生產情況;
8.生產管理、質量管理主要文件目錄;
9.藥品上市放行規程;
10.委托協議和質量協議;
11.持有人確認受托方具有受托生產條件、技術水平和質量管理能力的評估報告;
12.受托方相關材料
(1)受托方藥品生產許可證正副本復印件;
(2)受托方藥品生產企業的場地、周邊環境、基礎設施、設備等情況說明;
(3)受托方周邊環境圖、總平面布置圖、倉儲平面布置圖、質量檢驗場所平面布置圖;
(4)受托方生產工藝布局平面圖(包括更衣室、盥洗間、人流和物流通道、氣閘等,并標明人、物流向和空氣潔凈度等級),空氣凈化系統的送風、回風、排風平面布置圖,工藝設備平面布置圖;
(5)受托方空氣凈化系統、制水系統、主要設備確認或驗證概況;生產、檢驗儀器、儀表、衡器校驗情況;
(6)受托方主要生產設備及檢驗儀器目錄;
(7)受托方藥品出廠放行規程;
(8)受托方所在地省級藥品監管部門出具的通過藥品GMP符合性檢查告知書以及同意受托生產的意見;
13.申請材料全部內容真實性承諾書;
14.凡申請企業申報材料時,申請人不是法定代表人或負責人本人,企業應當提交《授權委托書》;
15.按申請材料順序制作目錄。
四、重要的先決條件:
1. 研發機構或企業;
2. 配備足夠的人員;
3. 建立完整的體系。
微信掃一掃
